Прионы, или жизнь без ДНК
Открытие прионов - величайшее достижение для науки вообще и биохимии в частности.
Их изучение началось в конце ХХ века. Тогда они считались лишь, не совсем обычно устроенными, белковыми молекулами, но постепенно открывались все новые стороны их жизни.
В прионах нет ни ДНК, ни РНК, и тем не менее они успешно размножаются. Настолько успешно, что представляют значительную опасность в некоторых случаях. Они подвержены мутациям и даже действию естественного отбора. Так что же они из себя представляют на самом деле?
Американский молекулярный биолог Стенли Б. Прузинер занимался изучением "скрейпи" - болезни овец, считавшейся вирусной. В 1982 году он впервые выделил ее возбудитель. Эта странная болезнь изучалась в течение нескольких десятилетий без видимого успеха. Ее отличительными признаками был особенно долгий инкубационный период и странности в пораженных тканях и органах. В конце 1950-х годов были обнаружены аналогии между болезнью "скрейпи" и заболеванием новогвинейского племени форе. Аборигены называли болезнь "куру", или "дрожь от сглаза", и приписывали ее возникновение колдовству. Причиной распространения куру в научном мире назван был ритуальный каннибализм.
После отказа от этого обычая болезнь практически перестала проявлять себя. Однако можно считать доказанным, что ее инкубационный период составляет более 30 лет, и отдельные случаи болезни связаны именно с долгим инкубационным периодом.Исследования этого заболевания принесли К.Гайдучеку Нобелевскую премию 1976 года.
Только в 1980-е годы благодаря стараниям С.Прузинера была установлена истинная природа обеих болезней.
Дело в правильной форме
.jpg)
Прионами называют молекулы белка PrP, если они свернуты необычным, неправильным образом. Название происходит от английского "proteinaceous infectious particles", то есть "белковые инфекционные частицы". Тот же белок PrP в обычной форме, или альфа-форме, не опасен, хотя его роль в живых организмах еще не до конца изучена. Доказано его существование в организмах всех млекопитающих, в том числе человека. Предположительно, его участие необходимо для ионного обмена или передачи нервных импульсов. Ряд ученых предполагает его важность для поддержания циклов активности и отдыха в течение суток. Исследователи пока не пришли к единому мнению, и все названные гипотезы нуждаются в проверке.
Более подробно изучен момент образования новых молекул белка. Прион имеет пространственную структуру PrP-Sc, при этом форма молекулы отлична от альфа-формы (нормы) и называется бета-формой. Если в момент синтеза рядом оказывается прион, формируется именно бета-форма. Другими словами, происходит размножение прионов. Открытие этой закономерности в научном мире признано настолько важным, что первооткрыватель явления Стенли Б. Прузинер в 1997 году был удостоен Нобелевской премии.
Механизмы этого влияния пока не изучены и при сегодняшнем уровне развития науки вряд ли могут быть объяснены в ближайшее время. Происхождение самих прионов также недостаточно ясно.
По одной из версий, в здоровом организме постоянно возникает небольшое число белковых образований из прионов, но они в короткие сроки распадаются. Если нарушен процесс "самоочищения клеток", белки неправильной формы накапливаются и возникают тяжелые болезни, порой с очень странными симптомами.
Прионы демонстрируют невероятную живучесть. Они устойчивы не только к стандартным методам дезинфекции, но и к особым биохимическим соединениям - протеолитическим ферментам. Именно эти ферменты отвечают за уничтожение старых или дефектных белковых молекул. Прионы с легкостью выдерживают кипячение, высушивание, замораживание, обработку спиртами и другими химически активными жидкостями, а также облучение ультрафиолетом и гамма-лучами. Можно сказать: когда погибает все живое, прион погибает последним.
Насколько они живые?
С момента, когда прионы были открыты и началось их глубокое изучение, исследователей волновал вопрос их эволюции. Распространяются ли на них законы эволюции по Дарвину? Точнее, существуют ли у прионов мутации, передающиеся по наследству? После ответа на этот вопрос требовалось бы определить, как мутации влияют на размножение прионов, оценить скорость этого процесса.
Только в середине двухтысячных годов исследователи смогли прийти к первым выводам. В результате серии экспериментов подтвердилась способность белка PrP сворачиваться в форму PrP-Sc несколькими различными путями. Подтверждено, что каждый из вариантов наследуется вполне устойчиво. Далее, проводились опыты по перенесении прионов от животных одного вида к другому. Полученные выводы говорят об уменьшении инкубационного периода у животных второго вида: следовательно, наблюдалась адаптация инфекционного агента. Измененный, "подстроившийся" под новые условия существования возбудитель болезни затем опять вводили животным первого вида, и в этом случае болезнь протекала иначе. Различия в симптоматике и ходе болезни подтверждали, что ее возбудитель видоизменился.
Другая серия опытов была посвящена изучению развития прионов в неблагоприятных условиях. В среду их обитания добавили вещество SWA, угнетающее прионы (служащее ингибитором для них). Жить и размножаться в таких условиях было сложнейшей задачей, но через некоторое время прионы продемонстрировали устойчивость к препарату SWA. С каждым новым поколением этих необычных белков их устойчивость только повышалась, и этот процесс справедливо сравнили с эволюцией.
По сравнению с дарвиновской эволюцией у прионов отсутствует классическая запись результатов, однако, тем не менее, они каким-то образом передают информацию по наследству. Пространственное строение белковой молекулы прионов не допускает большого разнообразия вариантов, что особенно заметно по сравнению с гигантскими возможностями ДНК.
Остается открытым вопрос о возникновении у прионов новых форм (видов) путем естественного отбора. Для ответа необходимо длительное изучение мелких изменений, которые либо будут закреплены, либо нет. Большинство ученых скептически относится к этой возможности, однако более глубокое изучение вопроса - дело ближайшего будущего.
Исключение из правил

Вероятно, не стоит ограничивать роль прионов только одним процессом. Инфекционные белки вполне могут быть частным случаем более серьезного явления. Если предположить, что в природе широко распространены белки с прионными качествами, то их влияние должно быть огромным. Ученые из университета Брукс в Оксфорде исследуют гипотезу, согласно которой исчезновение неандертальцев напрямую связано с прионами. Популяция была необратимо ослаблена, вероятно, в результате болезни, которую ученые назвали прионной инвазией. Возможно, она так же распространялась путем каннибализма, что уже рассматривалось на примере куру.
Возможно ли приспособиться к такой болезни, или неандертальцы были обречены? На этот вопрос частично отвечает статья американских ученых о событиях в племени форе ("Медицинский журнал Новой Англии", 2009). В последнее время среди представителей этого племени обнаружены случаи врожденной невосприимчивости к куру. Причиной возникшего иммунитета ученые считают новую форму гена Pr-nP, возникшую естественным путем в результате полиморфизма. Неясными все еще остаются многие моменты относительно того, как в данном случае работает иммунитет.
Прионы грибов (на примере дрожжей)
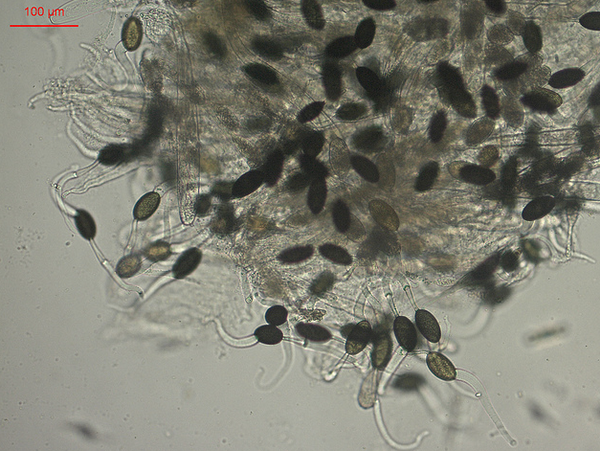
По сравнению с прионами млекопитающих, более всесторонне изучены прионы микромицетов, то есть микроскопических грибов. Их примером могут служить всем известные дрожжи.
Как развиваются прионы, например, дрожжей? Оказывается, в их образовании принимают участие белки - и нормальные, и в прионной форме. Особую роль играет HSP104, или белок теплового шока. Его обычное назначение - помогать белкам восстанавливать естественную форму после сильного воздействия, например, высоких температур. HSP104, который еще называют "шаперон", обладает тем же свойством, что и прионы: изменяет пространственную структуру других белков. В результате опытов установлено: если заблокировать действие шаперона, через короткое время из культуры грибов исчезнут все прионы.
Никакой опасности для человека прионы грибов представлять не могут, из-за серьезных отличий в строении с человеческими.
Роль прионов в болезни Альцгеймера
Болезнь Альцгеймера, как известно, поражает мозг. Нарушения в его работе вызываются появлением так называемых бляшек различной структуры, двух основных видов. Ученые из университетов Базеля и Кембриджа занимались исследованием взаимосвязей прионной инфекции с возникновением болезни Альцгеймера. Тау-белок измененной формы накапливается в нервных клетках и разрушает их. Как он появляется? Ученые дали ответ: обычный тау-белок превращается в дефектный, и этот процесс очень сильно напоминает прионную инфекцию.
Крупные бляшки относятся к бета-амилоидным, более мелкие состоят только из измененного тау-белка. В процессе образования нормального белка происходит сбой, из-за которого белковые цепочки распадаются на короткие участки, образуя бета-амилоидные бляшки. Тау-белок в нормальных условиях - часть цитоскелета, своеобразные внутренние "пути" или "рельсы" клетки, по которым двигаются органеллы. При болезни Альцгеймера тау-белок сворачивается в полимерные клубки, разрушая таким образом все пути внутриклеточного сообщения. Следующая стадия - исчезновение контактов между нейронами. Часто ситуацию ухудшает возникшее воспаление, вызванное ростом белковых полимеров: бляшек и клубков. Инфекционным агентом здесь служит сам белок, способ размножения которого не зависит ни от ДНК, ни от РНК и аналогичен способу размножения, присущее куру или скрейпи.
Изучение прионов и закономерностей их возникновения открывает новые научные горизонты и может заметно расширить возможности фармакологии и медицины.